靶向超声微泡造影剂的靶向类似于放射性药物、光学成像染料或磁共振成像(MRI)造影剂中的靶向,即将能够与目标受体(如靶细胞表面的疾病标记物)结合的特定配体附着在充满气体的超声微泡造影剂上。由此产生的靶向造影剂在患者或动物体内的血液中循环一段时间后逐渐被清除。由于特异的配体-受体相互作用,一些有机会流过靶标区域的靶向超声微泡造影剂被选择性地附着在受体上,因此使受体/疾病部位可以成像。本文我们将展示靶向性超声造影剂是如何监测如血栓形成、炎症、缺血/再灌注损伤、血管生成等相关疾病的。
要使微泡在动物体内给药后能与特定受体结合,就必须将靶向配体附着到微泡外壳上。附着可以通过共价或非共价手段来实现,也可以通过这些技术的组合来实现。那么制备中就需将将配体-聚合物/脂质偶联物(例如,生物素衍生物)添加到微泡脂质外壳原料中,而非微泡形成后添加。目前使用的许多配体都以生物素化的形式存在,只需将它们添加到链亲和素包被的微泡中,就会产生配体修饰的微泡。
配体修饰的微泡随着血流在脉管系统中移动:一小部分气泡会撞到物体上,比如携带特定受体的内皮细胞、白细胞或血凝块,这些都是分子成像的实际目标。研究微泡靶向性的最佳方法是在体外受控条件下,以已知的流速、配体和受体密度进行靶向性研究。平行板流动室通常用于这些研究。在流动的情况下,微泡上的配体与受体结合的时间非常有限。在极端情况下(大血管中1米/秒的血流),典型的配体与受体结合位点线性尺寸为1纳米时,必须在1纳秒内发生有效结合,这是一个极短的时间,与大多数抗体-抗原kon动力学常数不相容。自然界已经进化出快速结合的配体,在快速血流中与白细胞结合并缓慢滚动到活化的内皮,特别是存在于白细胞表面的p-选择素糖蛋白配体-1(PSGL-1)。低亲和力的单体唾液酰Lewisx和抗ICAM-1抗体结合在同一个气泡上,可以作为白细胞捕获的更现实的模拟,其中PSGL-1用于减慢白细胞的速度,然后ICAM-1配体在目标上实现细胞的完全捕获。通过在微泡壳上创造褶皱和额外的表面积,以模仿白细胞用于粘附内皮的延伸系绳的方式,可以在快速流动中进一步增强微泡与靶标的牢固粘附。
超声成像特有的一种增强微泡靶向性的技术与超声加压方法有关。值得注意的是,大多数微-气泡在穿过目标血管的过程中,可能会远离血管周边,几乎没有机会到达并选择性地结合内皮表面。垂直于流动方向的超声辐射的应用产生了初级辐射力,使颗粒转向靶区域,迫使它们在血管壁处停止,并使它们有更好的机会与目标结合并在停止超声波后保持与目标抗原的附着。即使是抗体靶向微泡也可以使用这种方法在高剪切流动条件下进行结合。
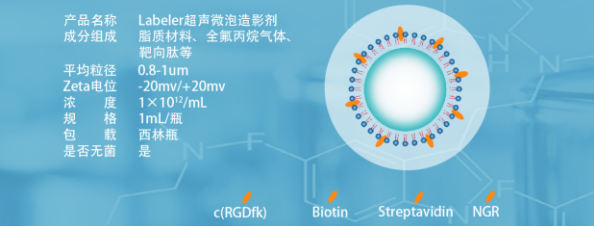
南京星叶生物自主研发了US-Star超声微泡造影剂系列,其中就包括多种靶向微泡,例如标记c(RGDfk)的Labeler R、标记链霉亲和素的Labeler S、标记生物素的LabelerB等。